Creado por el Laboratorio Castro.
1. Extracción de ADN
1.1 Materiales
- Placa petri
- Sonicador
- Bisturí
- Micropipeta (p1000, p200, p20)
- Guantes
- Buffer de lisis
- Lisozima (100 mg/µl)
- Tubo de molienda
- Beads
- Proteinasa K (200 mg/µl)
- SDS 10%
- Solución fenol-cloroformo-alcohol isoamílico
- Isopropanol
- Etanol 70%
- Pinzas
- Puntas micropipeta (p1000, p200, p20)
- Tijeras de podar
- Tubos (1.5 mL)
- Tubos (2 mL)
1.2 Procedimiento
Retirar con pinzas estériles el filtro de policarbonato (3 µm) del tubo Falcon y depositarlo en una placa de Petri. Utilizando un bisturí y una punta de micropipeta P1000, cortar el filtro en pequeños trozos y transferirlos a un tubo de 2 mL con beads de borosilicato (Merck, Z273619-1EA). Por lo general, el filtro mantiene gotas residuales de filtración; transfiera todo el líquido al tubo con beads.

Para colapsar la cubierta externa del filtro Sterivex (0.22 µm), se deben utilizar tijeras de podar previamente esterilizadas con etanol al 70%, partiendo desde el extremo de salida del filtro. Depositar el filtro en una placa de Petri estéril y utilizar un bisturí y una punta de micropipeta P1000 para cortar el filtro en pequeños trozos. Transferir los trozos a un tubo con beads. Al igual que con el filtro de 3 µm, el filtro Sterivex suele presentar líquido residual; transferir todo el volumen al tubo con beads.
Considerar el uso de campana o mechero durante el procedimiento.
Añadir 750 µL de buffer de lisis y 60 µL de lisozima (100 µL/mL) (Thermo Fisher, 89833) al tubo con los beads. Agitar inmediatamente en el vórtex a máxima velocidad durante 10 minutos. Luego, incubar los tubos a 40 °C durante 1 hora en el termobloque, agitando moderadamente en el vórtex cada 30 minutos.
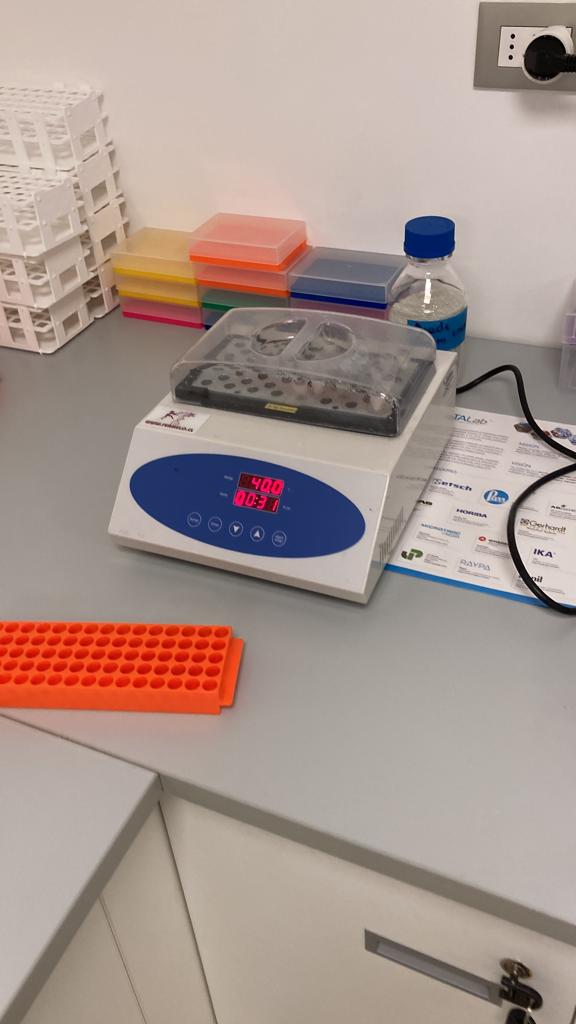
Retirar los tubos del termobloque, agregar 5 µL de proteinasa K (200 mg/mL) y 75 µL de SDS al 10%. Incubar nuevamente durante 1 hora a 55 °C, agitando con el vórtex suavemente cada 30 minutos.
Finalizada la incubación, centrifugar a 12.000 × g durante 5 minutos a 4 °C y transferir el sobrenadante completo a un tubo Eppendorf de 1.5 mL.
Agregar 500 µL de solución fenol:cloroformo:alcohol isoamílico (25:24:1), mezclar por inversión y centrifugar a 12.000 × g durante 5 minutos a 4 °C. Recuperar la fase acuosa superior y transferirla a un tubo Eppendorf de 1.5 mL.

Repetir la extracción con fenol:cloroformo:alcohol isoamílico. Agregar 500 µL de isopropanol frío (−20 °C) al tubo, mezclar por inversión e incubar toda la noche a −20 °C.
Centrifugar a 12.000 × g durante 25 minutos a 4 °C. Descartar cuidadosamente el sobrenadante y agregar 500 µL de etanol al 70%. Centrifugar a 12.000 × g durante 10 minutos a 4 °C. Descartar el etanol sin remover el pellet. Repetir el lavado con 500 µL adicionales de etanol al 70%.
Eliminar todo el remanente de etanol secando el tubo en el termobloque a 40 °C durante 40 minutos.
Resuspender el pellet en 60 µL de agua libre de nucleasas y cuantificar.
1.3 Preparación del buffer de lisis
En un shot estéril, mezclar:
- Xantogenato (Sigma 254770) — 1% p/v
- Acetato de amonio — 4 M
- Tris-HCl pH 7.4 — 10% v/v
- EDTA disódico 0.45 M pH 8 — 3.6% v/v
Completar con agua libre de nucleasas hasta el volumen final deseado. El buffer puede guardarse cubierto con papel aluminio a 4 °C por hasta 7 días.
